
Рефераты по рекламе
Рефераты по физике
Рефераты по философии
Рефераты по финансам
Рефераты по химии
Рефераты по хозяйственному праву
Рефераты по цифровым устройствам
Рефераты по экологическому праву
Рефераты по экономико-математическому моделированию
Рефераты по экономической географии
Рефераты по экономической теории
Рефераты по этике
Рефераты по юриспруденции
Рефераты по языковедению
Рефераты по юридическим наукам
Рефераты по истории
Рефераты по компьютерным наукам
Рефераты по медицинским наукам
Рефераты по финансовым наукам
Рефераты по управленческим наукам
психология педагогика
Промышленность производство
Биология и химия
Языкознание филология
Издательское дело и полиграфия
Рефераты по краеведению и этнографии
Рефераты по религии и мифологии
Рефераты по медицине
Учебное пособие: Анализ диаграмм состояния двойных сплавов
Учебное пособие: Анализ диаграмм состояния двойных сплавов
РАБОТА 5
АНАЛИЗ ДИАГРАММ СОСТОЯНИЯ ДВОЙНЫХ СПЛАВОВ
Цель работы: изучение основных типов диаграмм состояния двойных систем, приобретение практических навыков изучения превращений, протекающих при кристаллизации сплавов, анализ полученных данных и определение возможности их использования па практике.
Знание диаграмм состояния различных систем, характеризующих превращения в сплавах, и умение анализировать эти превращения позволяют оценить свойства сплавов и в конечном итоге рационально выбрать материал для тех или иных изделий в зависимости от предъявляемых к ним требований.
Диаграммы состояния изображаются в координатах температура - содержание компонентов. Линии, соединяющие критические точки аналогичных превращений в системе, разграничивают области существования равновесных фаз. Любая точка на диаграмме определяет фазовый и химический составы сплава, а также его структуру при данной температуре. Вертикальная линия соответствует определенному химическому составу сплава. В зависимости от того, как взаимодействуют компоненты сплавов между собой в твердом состоянии (обладают различной взаимной растворимостью и образуют твердые растворы; образуют эвтектики или химические соединения), различают несколько типов диаграмм.
Рассмотрим, например, превращения, происходящие в сплавах Al - Са (рис. 5.1). Выше линии ликвидус ABCDEF оба компонента находятся в жидком состоянии и в любых соотношениях неограниченно растворяются друг в друге. Ниже линии солидус AMBNPQKEH сплавы системы находятся в твердом состоянии. Фнализ диаграммы показывает, что при затвердевании происходят следующие превращения.
1. Образуется α -твердый раствор Са в А1. Область существования твердого раствора – AMS1 прилегает к линии чистого А1. Точка М показывает максимальную растворимость Са в А1, точка S1 — минимальную, линия MS1 — ограничение растворимости Са в Al. Итак, с понижением температуры наблюдается уменьшение растворимости Са в Al в соответствии с линией MS 1. Избыточный кальций, который не может быть растворен в α - твердом растворе, выделяется при охлаждении ниже линии MS1 в виде вторичных кристаллов СаAl 3 11 в отличие от первичных СаAl 3, образующихся при наличии жидкой фазы в точке Р.
2. Образуются химические соединения СаAl3 и СаAl 2, кристаллизующиеся из жидкого сплава при температурах, соответствующих точке D, и точке Р при взаимодействии жидкой фазы и химического соединения СаAl2 (соответственно) .
Превращение, протекающее при постоянной температуре, когда из двух фаз, одна из которых является жидкой, образуется третья и все фазы в момент превращения имеют определенный состав, называется перитектическим и может быть записано в виде реакции
T= const
Ж c + CaAl 2 (Q) ———-> СаА1 3(р),
где символы С, Q, Р показывают содержание компонентов в соответствующих фазах.
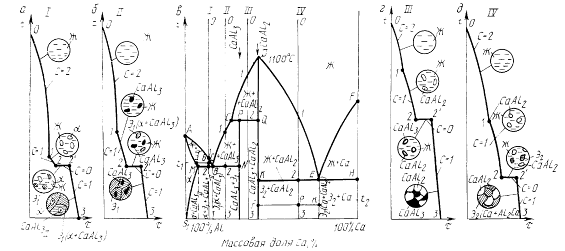
Рис. 5.1. Диаграмма состояния (в) и кривые охлаждения (а, б, г, д) сплавов системы Al - Са (структурный анализ):
I...IV — номера сплавов
В процессе перитектического превращения в соответствии с правилом фаз С = К – Ф + 1 = 2 3 + 1 = 0. Применение правила отрезков (конода CPQ) показывает, что при перитектическом превращении массы взаимодействующих фаз строго определенны. В доперитектических сплавах, расположенных левее точки Р, в избытке остается жидкая фаза, которая затем испытывает все превращения, описанные ниже для сплава II. В заперитектических сплавах, расположенных правее точки Р, избыточной является твердая фаза (в данном случае СаAl2). Химическое соединение СаAl3 является устойчивым при нагревании вплоть до температуры плавления (точка D). Химическое соединение СаAl3 неустойчиво и, будучи нагретым до температуры точки Р, разлагается на жидкость и СаAl2.
3. Формируются две эвтектики Э 1 и Э 2. Первая представляет собой тонкую механическую смесь кристаллов α -твердого раствора и СаА1 3, образующуюся (при С = 0) из жидкости по реакции
![]()
Вторая эвтектика представляет собой тонкую механическую смесь кристаллов Са и СаAl 3 и образуется но реакции
![]()
При этом превращении, как и при первом эвтектическом превращении, система нонвариантна (С = 0).
В ряде систем возможна подобная реакция, но смесь двух различных фаз образуется не из жидкости, а из твердого раствора. Такая реакция называется эвтектоидной.
Рассмотрим кривые охлаждения нескольких сплавов (см. рис. 5.1) и проведем их подробный структурный анализ.
Сплав I. При охлаждении от точки 0 до точки 1 (см. рис. 5.1, а) сплав находится в жидком состоянии (С = 2). При температуре t 1, соответствующей точке 1, начинается кристаллизация сплава. Конода abc—отрезок изотермы, проведенный влево и вправо от линии сплава до пересечения с линиями диаграммы, где расположены искомые фазы или структурные составляющие (см. рис. 5.1, в). Она показывает, что это кристаллы α - твердого раствора (точка а коиоды указывает на область α ). Вторая точка коноды с указывает на наличие жидкой фазы. Пользуясь правилом отрезков, можно определить массовую долю (Q, %) сосуществующих фаз. Например, при температуре t 1 Q α = bc / ac*100, Q ж = bc / ac*100. Итак, для определения содержания любой из двух фаз необходимо взять отношение длины противолежащего от искомой фазы отрезка коноды к длине всей коноды. Проекции точек а и с на ось концентраций покажут, каково содержание компонентов в каждой из фаз (точка а — в α - твердом растворе, точка с — в жидкой части сплава).
При охлаждении сплава I от t 1 до t 2 доля твердой фазы растет, а жидкой соответственно уменьшается, что подтверждается правилом отрезков.
К моменту охлаждения сплава до t 2 содержание компонентов в последних порциях кристаллов α - твердого раствора будет соответствовать точке М, а в жидкости — точке В. Как видно, жидкость имеет эвтектический состав и потому она кристаллизуется по первой эвтектической реакции (С = 0), протекающей при постоянной температуре (t2 = t 2’). С исчезновением при t 2’ жидкости первичная кристаллизация заканчивается, а от t 2’ до t 3 протекает вторичная кристаллизация сплава (из твердой α - фазы выделяется СаAl 3 11).
Сплав II. От t 0 до t 1 (см. рис. 5.1, б) идет охлаждение жидкой фазы, от t 1 до t2 - выделение из жидкости кристаллов СаAl3. Затем протекает эвтектическая реакция при постоянной температуре (линия MBN на рис. 5.1, в) и жидкая часть сплава переходит в эвтектику. Ниже t 2 никаких превращений в кристаллах СаAl 3 и в эвтектике не происходит.
Сплав III. От t 0 До t 1 (см. рис. 5.1, г) идет охлаждение жидкой фазы, от t 1 до t 2 происходит выделение из жидкости кристаллов CaAl 2. По достижении температуры, соответствующей линии CPQ, протекает перитектическая реакция (С = 0)
![]()
Поскольку линия сплава III проходит правее точки Р, т. е. ближе к линии CaAl 2, то в результате перитектического превращения образуется СаAl3 и некоторая часть СаAl2 остается в избытке. Ниже t 2 никаких превращений в сплаве не происходит.
Кристаллизацию сплава IV (см. рис. 5.1, д) анализируют по аналогии с рассмотренными выше сплавами.
Анализ кривых охлаждения чистых компонентов Al и Са и химического соединения CaAl2 показывает, что они имеют одинаковый характер (площадку кристаллизации в точках A, F и D соответственно) и отличаются лишь температурным уровнем площадки кристаллизации. Таким образом, устойчивые химические соединения ведут себя подобно компонентам сплава и, приняв CaAl 2 условно за компонент, диаграмму А1—Са (см. рис. 5.1, в)
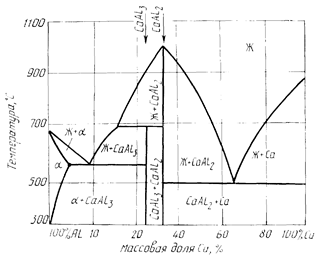
Рис. 5.2. Диаграмма состояния сплавов системы Al - Са (фазовый анализ)
Можно рассматривать как состоящую из двух самостоятельных диаграмм А1—CaAl2 и СаAl2 — Са. При этом диаграмма CaAl 2 — Са является по существу элементарной диаграммой, когда оба компонента в твердом состоянии нерастворимы друг в друге и образуют механическую смесь—эвтектику. Аналогичная диаграмма (Sn—Zn) была рассмотрена в работе 4. Диаграмма А1—CaAl 2 состоит из частей элементарных диаграмм состояния с ограниченной растворимостью компонентов в твердом состоянии, с эвтектическим и перитектическим превращениями.
На рис. 5.2 приведены результаты фазового анализа диаграммы Al Са.
Фазовый состав сплавов в любой области легко определить с помощью коноды, концы которой указывают на равновесные сосуществующие фазы и содержание в них компонентов. Линия ликвидус показывает не только температуру начала кристаллизации соответствующих сплавов, но и содержание компонентов в жидкой фазе любого сплава в зависимости от температуры. Солидус определяет температуру окончания кристаллизации и содержание компонентов в твердой кристаллизующейся фазе.
В случае, если необходимо определить массовую долю структурных составляющих, например, в сплаве IV для температуры t 2 — эвтектики и СаАl 2, проводят коноду fpk (см. рис. 5.1) до линий, соответствующих составляющим, и пользуются соотношениями Q CaAl 2 = ph / (fh) * 100 и Qэ 2 = fh / 9fk)*100. Структурная составляющая сплава имеет под микроскопом своеобразный вид.
Задания
1. Начертить заданную преподавателем диаграмму состояния двойных сплавов (см. прил. 2.1—2.24).
2. Обозначить все линии диаграммы, отметив линии ликвидус и солидус.
3. Провести структурный и фазовый анализ диаграммы и описать все нонвариантные превращения в сплавах.
4. Построить кривую охлаждения для заданного преподавателем сплава с объяснением всех превращений и зарисовкой микроструктур, с применением правила фаз и правила отрезков (для двух различных фазовых областей).
5. Сделать выводы и написать отчет по работе в соответствии с пунктами заданий.
Занятие в подгруппе целесообразно посвятить разбору нескольких реальных характерных диаграмм состояния, а индивидуальное задание рекомендовать выполнить дома.
Процесс структурообразования в сплаве IV студенту рекомендуется описать самостоятельно, используя кривую охлаждения этого сплава, приведенную на рис. 5.1.
© 2009 База Рефератов